Die ISO-18562-Normenreihe wird verwendet, um die Biokompatibilität von Medizinprodukten mit einem Atemgasweg zu bewerten, insbesondere im Hinblick auf potenziell gefährliche Substanzen, denen der Patient über den Gasstrom ausgesetzt sein kann.
Alle Teile von ISO 18562 wurden 2024 aktualisiert und führen mehrere neue Testanforderungen für Hersteller von CPAP-Geräten und Anästhesiemaschinen, Beatmungsgeräten, Befeuchtern, Überdruckkammern und anderen Medizinprodukten mit einem atemfähigen Gasstrom ein. Zu den wichtigsten Änderungen gehören ein erweitertes Spektrum flüchtiger organischer Verbindungen, die analysiert werden müssen, sowie die Anforderung, das Kondensat-Volumen zu bestimmen, das über das Gerät zum Patienten gelangen kann.
Ab dem 5. Juli 2026 müssen alle neuen Voranmeldungen bei der FDA auf die überarbeiteten Versionen der ISO-18562-Normen verweisen.1 Ebenso sind die Ausgaben von 2024 in der EU nun als harmonisierte Normen anerkannt, was bedeutet, dass das Testen neuer Geräte gemäß diesen Normen der direkteste Weg ist, die Konformität mit den relevanten Teilen der EU-MDR nachzuweisen.2
Dieser Artikel fasst alle vier Teile der aktualisierten ISO-18562-Normenreihe zusammen, mit einem Schwerpunkt auf den praxisrelevanten Aspekten der Prüfung für Hersteller von Medizinprodukten.
ISO 18562-1: Bewertung und Prüfung im Rahmen eines Risikomanagementprozesses
ISO 18562-1:2024 entspricht in etwa ISO 10993-1:2025 und beschreibt die allgemeinen Grundsätze für Biokompatibilitätstests und Risikobewertungen, insbesondere für Gaspfade, da diese von der ISO-10993-Reihe nicht ausreichend abgedeckt werden.
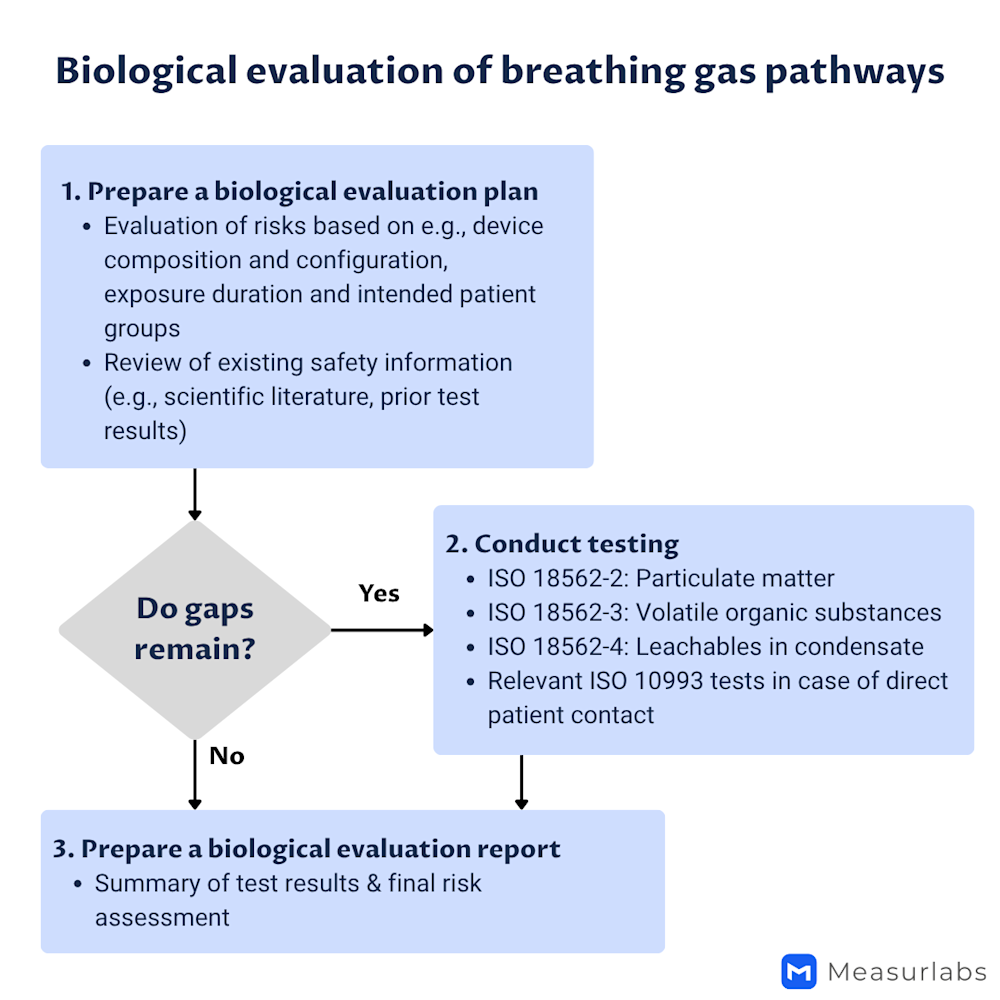
Der Umfang der biologischen Bewertung gemäß ISO 18562-1 hängt von der Kategorisierung des Gaswegs, den damit verbundenen Risiken und dem Ausmaß ab, in dem diese Risiken durch vorhandene Daten abgedeckt werden. Der Prozess verläuft in der Regel in folgender Reihenfolge:
Identifizierung von Biokompatibilitätsrisiken im Zusammenhang mit der Materialzusammensetzung, der physischen Konfiguration und den Leistungsmerkmalen des Geräts.
Bewertung der Risiken durch diese Gefährdungen für den Patienten, basierend auf der vorgesehenen Gesamtexpositionsdauer und der Patientengruppe.
Erstellung eines biologischen Bewertungsplans (BBP), in dem die identifizierten Gefährdungen und Risiken sowie vorhandene unterstützende Nachweise (z. B. wissenschaftliche Literatur oder frühere Testdaten) dokumentiert werden.
Identifizierung von Lücken, die durch vorhandene Daten nicht ausreichend abgedeckt werden, sowie Auswahl geeigneter Tests zur Schließung dieser Lücken.
Prüfung gemäß Teil 2, Teil 3 und/oder Teil 4 der ISO 18562 sowie weiterer relevanter Normen, wie vom BEP gefordert.
Erstellung eines biologischen Bewertungsberichts (BER), der die Testergebnisse und das Ergebnis der abschließenden Risikobewertung zusammenfasst.
Kategorisierung von Gaspfaden gemäß ISO 18562-1
Expositionskategorie | Expositionsdauer* |
Begrenzte Exposition | ≤ 24 h |
Längere Exposition | > 24 h, aber ≤ 30 d |
Langzeitexposition | > 30 d |
* Bei mehrfacher Verwendung desselben Geräts am selben Patienten umfasst dies den gesamten Expositionszeitraum über alle vorgesehenen Anwendungen.
Neben der Expositionsdauer beeinflusst die Patientengruppe die tolerierbare Exposition (TE) gegenüber gefährlichen Substanzen. Die neueste Version der ISO 18562-1 enthält sechs Patientengruppen: Erwachsene, Jugendliche, Kinder, Kleinkinder, Säuglinge und Frühgeborene, jeweils mit einem eigenen täglichen Atemvolumen, das zur Berechnung der maximalen TE-Werte für flüchtige organische Substanzen und Auslaugprodukte verwendet wird.
ISO 18562-2: Prüfungen auf Emissionen von Partikeln
ISO 18562-2 legt die Tests und Akzeptanzkriterien zur Bewertung der Patientenexposition gegenüber Partikeln über den Gaspfad eines Medizinprodukts fest. Um die Norm zu erfüllen, dürfen Atemgaswege den Patienten keinen Partikelkonzentrationen aussetzen, die die folgenden Grenzwerte überschreiten:
12 µg/m3 für Partikel mit einem Durchmesser ≤ 2,5 µm (PM2,5)
150 μg/m3 für Partikel ≤ 10 µm Durchmesser (PM10)
Die Norm beschreibt mehrere alternative Prüfmethoden zur Messung von Partikelemissionen:
Einfach- und Doppelfilter-Setups: Ein Gasstrom wird durch das Medizinprodukt geleitet, und am Ausgangsstrom wird ein Partikelfilter platziert, um alle Partikel mit einem Durchmesser > 0,25 µm aufzufangen. Da die Partikelgrößen darüber hinaus nicht differenziert werden, beträgt der Konformitätsgrenzwert für alle aufgefangenen Partikel 12 µg/m3.
Wenn für den Einzelfiltertest keine ausreichend saubere Luft verfügbar ist, kann ein weiterer Filter in den Eingangsluftstrom eingesetzt werden. Die Differenz der Partikelkonzentrationen an den verschiedenen Filtern wird dann berechnet, um die Menge der vom Medizinprodukt abgegebenen Partikel zu ermitteln.
Filtermethode mit partikelgrößenbasierter Trennung: Neben Filtern umfasst der Versuchsaufbau einen Trägheits-Partikelgrößenabscheider, der Partikel in Fraktionen unter 10 µm und unter 2,5 µm trennt, sodass die Konzentrationen mit den oben aufgeführten größenabhängigen Grenzwerten verglichen werden können.3
Partikelzähler-Methode: Die Partikelanzahl nach Größenbereich wird im Ausgangsstrom mithilfe eines kalibrierten Partikelzählers gemessen. Die Ergebnisse werden anschließend in Massenkonzentrationen umgerechnet und mit den Grenzwerten verglichen.
ISO 18562-3: Prüfungen auf Emissionen flüchtiger organischer Substanzen
ISO 18562-3 legt Tests für die Emissionen flüchtiger organischer Substanzen (VOS) fest, die vom Patienten bei der Verwendung der Gaswegvorrichtung eingeatmet werden können. Die vorherige Ausgabe bezog sich auf flüchtige organische Verbindungen (VOC), jedoch wurde die Terminologie für die Version 2024 aktualisiert, um neben VOC auch schwerflüchtige und sehr flüchtige organische Verbindungen (SVOC und VVOC) einzuschließen.
Beim ISO 18562-3-Test wird das Medizinprodukt in einer Testkammer aufgebaut, auf der höchsten vorhersehbaren Anwendungstemperatur gehalten und mit der niedrigsten klinisch relevanten Durchflussrate betrieben, da diese Bedingungen zur ungünstigsten Inhalationsdosis führen. Die durch das Gerät geleitete Luft wird beprobt und mittels einer GC-MS-Methode analysiert, um die VOC-Konzentrationen in µg/m3 zu identifizieren und zu messen.
Die Ergebnisse für jede Substanz werden anschließend mit den maximal zulässigen Expositionsgrenzwerten verglichen, die aus toxikologischen Daten und den in ISO 18562-1 festgelegten standardmäßigen täglichen Atemvolumina für verschiedene Patientengruppen abgeleitet werden. Für die Berechnungen wird die ungünstigste vorgesehene Patientengruppe herangezogen (d. h. diejenige, die zur niedrigsten zulässigen Konzentration führt).
ISO 18562-4: Tests auf auslaugbare Stoffe im Kondensat
ISO 18562-4 beschreibt Tests zur Bewertung von Substanzen, die sich in Kondensat im Atemgasweg lösen und über diesen den Patienten erreichen könnten. Das Verfahren ist wie folgt:
Der erste Schritt besteht darin, das Volumen des flüssigen Kondensats zu bestimmen, das den Patienten innerhalb von 24 Stunden erreichen kann, wenn das Gerät unter klinisch relevanten Worst-Case-Parametern betrieben wird. Wenn nachgewiesen werden kann, dass nicht mehr als 0,1 ml Kondensat den Patienten innerhalb von 24 Stunden erreichen, sind keine weiteren Tests erforderlich.
Wenn das Kondensatvolumen größer ist, besteht der nächste Schritt darin, auslaugbare Stoffe im Kondensat mithilfe verschiedener analytischer Methoden zu identifizieren und zu quantifizieren (GC-MS und LC-MS für organische auslaugbare Stoffe sowie ICP-MS für anorganische Elemente) – gemäß ISO 10993-18.
Die gemessenen Auswaschkonzentrationen werden mit substanzspezifischen tolerierbaren Aufnahmegrenzen verglichen, die auf Grundlage der ISO 18562-1 für organische Auswaschstoffe und der ICH-Q3D-Richtlinie für anorganische Auswaschstoffe berechnet werden.
Wenn die tolerierbare Aufnahme für einen Stoff überschritten wird, ist eine toxikologische Risikobewertung gemäß ISO 10993-17 erforderlich.
Unsere Lösungen für die Prüfung von Atemgaswegen
Measurlabs bietet das vollständige Spektrum an Analysen, die für die Biokompatibilitätsbewertung von Atemgaswegen gemäß ISO 18562 erforderlich sind. Wenn das Gerät Teile enthält, die in direkten Kontakt mit dem Patienten kommen, kann das Prüfprogramm um die relevanten ISO 10993-Tests erweitert werden.
Wir empfehlen, den Prozess mit der Erstellung eines biologischen Bewertungsplans (BEP) zu beginnen, da dieser die erforderlichen Tests für das jeweilige Gerät festlegt. Falls Sie noch keinen BEP haben, können wir Ihnen bei der Erstellung helfen. Bitte kontaktieren Sie unsere Experten über das untenstehende Formular, um Ihre Testanforderungen zu besprechen und ein individuelles Angebot zu erhalten.
Quellenverzeichnis
1 Siehe FDA's Recognized Consensus Standards Database: ISO 18562-1:2024
2 Siehe Durchführungsbeschluss (EU) 2026/193 der Kommission
3 Diese Methode wird ausführlich in den Anhängen J und L des 40 § CFR Part 50 der US-amerikanischen Umweltschutzbehörde (EPA) beschrieben.